CH3OH燃料电池方程式
来源:学生作业帮助网 编辑:作业帮 时间:2024/05/11 17:18:33
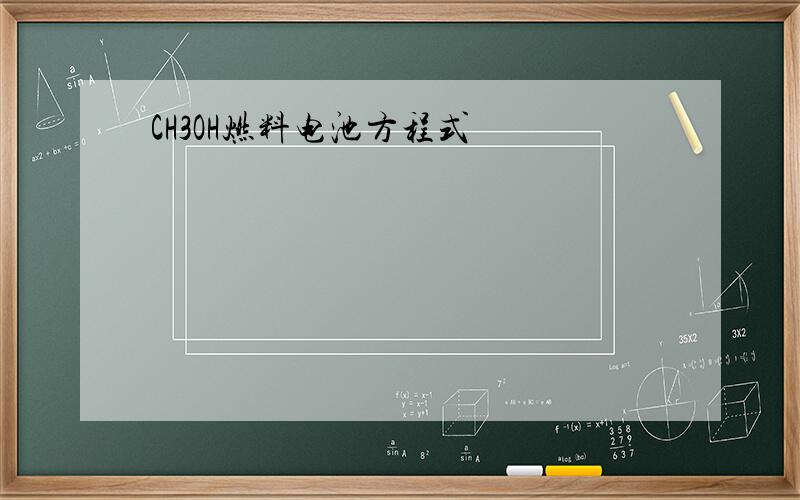
总反应Li+FePO4=LiFePO4负极:Li+e-=Li+正极:FePO4+e-+Li+=LiFePO4总反应2CH3OH+3O2+4OH-=2CO32-+6H2O正极:3O2+12e-+6H2O
酸性条件下加不加都一样总反应方程式不变看正极反应就知道了其实是加的只是在负极中一样得到了所以总反应方程式不用写碱性条件下正极得到12个OH–负极失去16OH~所以总反应方程式要写
CH3OH+H2O-6e====CO2+6H+O2+4H++4e====2H2O
我认为应该这样写:2CH3OH-12e-+16OH-=2CO3^2-
氢氧燃料电池电极反应方程式(1)碱性介质负极:2H2-4e-+4OH-=4H2O正极:O2+4e-+2H2O=4OH-(2)酸性介质负极:2H2-4e-=4H+正极:O2+4e-+4H+=2H2O甲烷
碱性氢氧燃料电池正极反应式:O2+4e-+2H2O==4OH-,负极:2H2-4e-+4OH-==2H2O.
需要因为负极反应的反应物没有气体生成物有气体
【碱性电解质】正极:O2+4e-+2H2O=4OH--负极:2NH3-6e-+6OH-=N2+6H2O保证正负极得失电子相同,正极乘以3+负极乘以2得答案4NH3+3O2=2N2+6H2O方法二:一般
氢氧燃料电池以碱为电解质放电反应正极(O2)反应式:O2+2H2O+4e-=4OH-(还原反应),负极(H2):2H2-4e-+4OH-=4H2O(氧化反应)总反应:2H2+O2=2H2O1、燃料电池
直接甲醇燃料电池(DirectMethanolFuelCell),它属于质子交换膜燃料电池(PEMFC)中之一类,系直接使用水溶液以及蒸汽甲醇为燃料供给来源,而不需通过重组器重组甲醇、汽油及天然气等再
这个问题很简单,就是电荷守恒问题.因为甲醇中的C是-2价,被氧化生成CO32-,其中C+4价,失去6e-,C守恒,则有1CH3OH-6e-+OH-----》1CO32- +H2O再根据电荷守恒,电子呈
甲烷电池负极:CH4+10OH-—8e-===CO32-+7H2O正极:O2+4e-+2H2O===4OH-乙烷电池负极2CH3CH3-28e-+36OH-====4CO32-+24H20正极7O2+
一般来说,写燃料电池反应,可以先写正极反应(一般都是氧气)和总反应.然后通过总反应减去正极,得出负极的电极反应.总反应还要看电解质溶液为酸性还是碱性,一般碱性的居多.如果为酸性电解质溶液,总反应就为这
正极2O2+4H20+8e-=8OH-负极CH4-8e-+10OH-=CO32-+3H2O
CH3OH中C是相当于-2价,升到CO3^2-,要升6价,转移6个电子.然后CH3OH前面系数是2,加起来就是12个电子.氢氧根数要让正负价相等就可以
负极2CH3OH+16OH--12e-=2CO32-+12H2O正极3O2+6H2O+12e-=12OH-总2CH3OH+3O2+4OH-=2CO32-+6H2O
在酸性介质,负极:CH3OH-6e-+H2O=CO2+6H+正极:O2+4e-+4H+=2H2O在碱性介质负极:CH3OH-6e-+8OH-=CO32-+6H2O正极:O2+4e-+2H2O=4OH-
我们一般使用的是碱性燃料电池,反应式为 负极:CH4+10OH--8e-=CO3²﹣+7H2O 正极:2O2+4H2O-+8e-=8OH- 总方程式:CH4+2O2=CO2+2H2OC
负极:2CH3OH-12e–+2H2O=12H++2CO2;负极发生氧化反应正极:3O2+12e–+12H+=6H2O正极发生还原反应再问:哪来的氧气这道题可没说加氧气.再答:氧化需要氧气参加
以甲烷燃料电池为例(1)电解质是H2SO4溶液总反应 CH4+2O2=CO2+2H2O正极 2O2+8e-+8H+ =4H2O 负极 CH