32.5g的锌粒与280g硫酸溶液恰好完全反应.求(1)生成氢气多少克?(2)所用硫酸溶液的溶质的质量分数是多少?
来源:学生作业帮 编辑:搜狗做题网作业帮 分类:化学作业 时间:2024/05/09 05:32:26
32.5g的锌粒与280g硫酸溶液恰好完全反应.求(1)生成氢气多少克?(2)所用硫酸溶液的溶质的质量分数是多少?
(3)生成物溶液的溶质的质量分数是多少?
(3)生成物溶液的溶质的质量分数是多少?
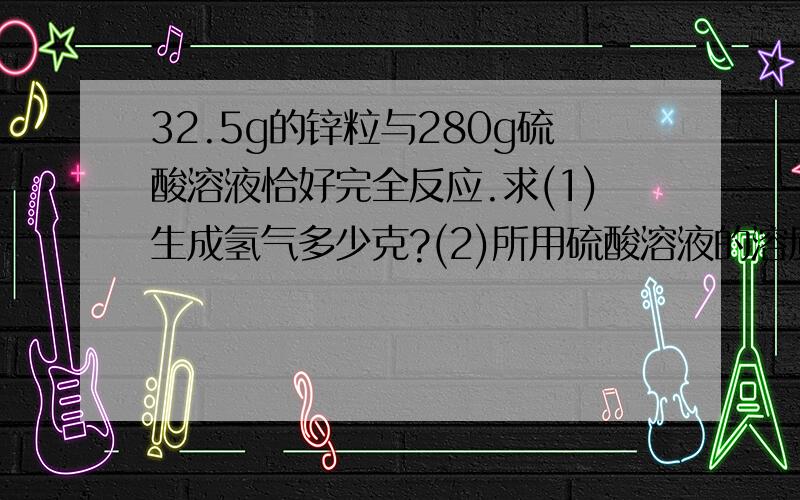
Zn+H2SO4=ZnSO4+H2(气体)
65 98 161 2
32.5g y z x
硫酸过量,锌全部反应
65/2=32.5g/x
x=1g;
65/98= 32.5g/y;
y=49g;
65/161=32.5g/z;
z=80.5g
(1).生成氢气的的质量是1g;
(2).所用硫酸溶液的溶质的质量分数是:49g/280g*100%=17.5%;
(3).生成物溶液的溶质的质量分数是:80.5g/(32.5g+280g-1g)*100%=25.8%
再问: 我不明Y跟Z的求法,能不能讲一下?
再答: Zn+H2SO4=ZnSO4+H2(气体) 65 98 161 32.5g y z 65/98= 32.5g/y; y=49g; 65/161=32.5g/z; z=80.5g
再问: 我觉得你写错了,不过还是谢谢你!
65 98 161 2
32.5g y z x
硫酸过量,锌全部反应
65/2=32.5g/x
x=1g;
65/98= 32.5g/y;
y=49g;
65/161=32.5g/z;
z=80.5g
(1).生成氢气的的质量是1g;
(2).所用硫酸溶液的溶质的质量分数是:49g/280g*100%=17.5%;
(3).生成物溶液的溶质的质量分数是:80.5g/(32.5g+280g-1g)*100%=25.8%
再问: 我不明Y跟Z的求法,能不能讲一下?
再答: Zn+H2SO4=ZnSO4+H2(气体) 65 98 161 32.5g y z 65/98= 32.5g/y; y=49g; 65/161=32.5g/z; z=80.5g
再问: 我觉得你写错了,不过还是谢谢你!
32.5g的锌粒与280g硫酸溶液恰好完全反应.求(1)生成氢气多少克?(2)所用硫酸溶液的溶质的质量分数是多少?
15克锌与100克稀硫酸溶液恰好完全反应,求反应后生成氢气质量多少?稀硫酸溶液中溶质的质量分数是多少?
4.8g放入100g稀硫酸溶液中,恰好完全反应1生成氢气多少克2这种稀硫酸溶液中溶质的质量分数3反应后生成的溶液中溶质的
一定量的锌和100g的稀硫酸恰好完全反应,生成1g的氢气,求生成溶液的溶质质量分数.
6.5g锌与100g的稀硫酸恰好完全反应 试计算:1 生成氢气的质量 2 稀硫酸溶质的质量分数.3 反应后形成溶液中溶质
200g某硫酸溶液恰好与锌完全反映,生成0.4g氢气,试计算:(1)该硫酸溶液的溶质质量分数是多少?(2)要配置该溶质质
若将13g锌放入100g稀硫酸溶液中恰好完全反应,则可生成氢气多少克?参加的稀硫酸中溶质的质量分数是多少?
32.5g金属锌与一定质量的溶质质量分数为10%的稀硫酸恰好完全反应,生成氢气质量多少,反应后溶液中溶质的
在4g锌与100g稀硫酸充分反应后生成0.2g氢气,(1)计算所用稀硫酸中溶质的质量分数(2)生成物的溶液中的质量分数
6.5g锌与100g稀硫酸恰好完全反应.求:(1)稀硫酸溶液中溶质的质量分数.(2)反应后溶液中溶质的质量分数.
铜和锌的混合物10g与100g稀硫酸恰好完全反应,生成0.2g氢气.求该稀硫酸中溶质质量分数.
如果32.5g锌恰好能和200g稀硫酸完全反应.原稀硫酸溶液的溶质的质量分数是多少?求计算过程和思路.